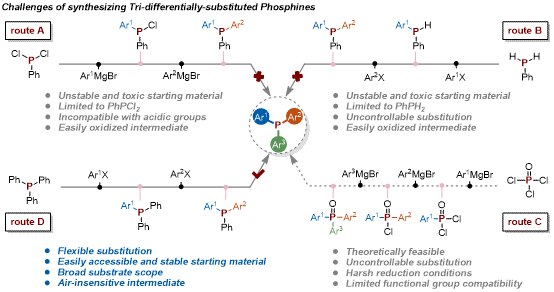
过渡金属催化领域的许多最新进展都是由特定的辅助配体推动的,这些配体能够以前所未有的方式调节催化剂的反应活性。多芳基叔膦作为很多反应中的首选配体,其具有一个显著的优点,即可以通过改变磷中心的取代基来精确调整配体的电子和空间特性。传统上,多芳基叔膦可以通过卤代膦底物与有机金属试剂的亲核取代反应合成。此外,还可通过膦氢试剂与有机卤化物的交叉偶联反应合成多芳基叔膦。然而,上述反应合成步骤较为繁琐,涉及难以分离的有毒或自燃试剂以及对空气敏感的中间体,这使得多芳基叔膦的制备变得较为困难。且均无法实现叔膦连接基团的第三次改性。理论上可以三氯氧膦出发经由三次连续亲核取代反应合成多芳基叔膦,但是该方法仍然受限于过度反应与苛刻的还原条件。
近日,大连理工大学金云鹤副教授和清华大学付华教授合作,依托课题组扎实的光化学研究基础(Nat. Commun. 2024, 15, 8619; Angew. Chem. Int. Ed., 2022, 61, e202204918; JACS Au 2024, 4, 4899; ACS Catal. 2025, 15, 3306; J. Am. Chem. Soc. 2017, 139, 14237),在该领域取得了突破性进展,通过五配位的膦中心EDA复合物,经由单电子转移选择性断裂C−P键构建多芳基叔膦。
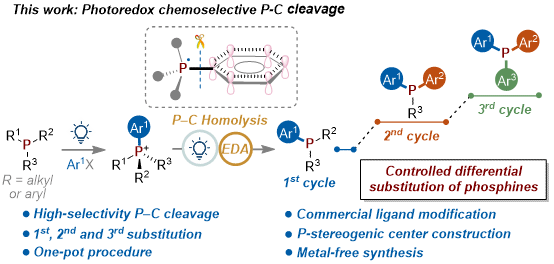
该反应方法显示出良好的底物适用范围,该反应无需金属和保护基的参与,首次实现同一膦分子上连续三次可控芳基化,从PPh3出发经三步获得三异芳基膦7(总收率26%),消除过渡金属残留,对药物分子的合成至关重要。

相关机理研究证明化学选择性C−P键切断的选择性来源为键能不同,经DFT计算发现电子效应主导选择性:缺电子芳基>苯基>富电子芳基>烷基。

该工作以“Tertiary Phosphine Diversification via Photochemical P−C Chemoselective Cleavage of Phosphonium Salt”为题发表在《Angew. Chem. Int. Ed.》上。化学学院的博士研究生甘子玉,硕士研究生陈家劲与贺海龙为共同第一作者。清华大学付华教授和大连理工大学化学学院金云鹤副教授为共同通讯作者,大连理工大学为第一完成单位。